Information om Region Hallands arbete med medicinteknik generellt finns på sidan Medicinteknik (vardgivare.regionhalland.se)
Nationellt ordnat införande av medicinteknik
Genom nationellt ordnat införande samverkar alla Sveriges regioner för att uppnå en jämlik, kostnadseffektiv och ändamålsenlig användning av nya medicintekniska produkter över hela landet. Det medicintekniska produktrådet, MTP-rådet, utser vilka medicintekniska produkter som ingår i nationell samverkan och ger rekommendationer om hur de bör införas och användas.
Nationellt ordnat införande drivs inom ramen för Regionernas samverkansmodell för medicinteknik som är en del av det nationella systemet för kunskapsstyrning inom hälso- och sjukvården. Inom samverkansmodellen ingår även en beredningsgrupp som bereder och följer upp regionernas gemensamma agerande.
MTP-rådet och dess beredningsgrupp är utsedda av de sex samverkansregionerna för hälso- och sjukvård. Regionernas samverkansmodell för medicinteknik koordineras och förvaltas av SKR på uppdrag av samtliga regioner och arbetet sker i samarbete med Tandvårds- och läkemedelsförmånsverket, TLV. Nationellt ordnat införande bygger också på ett nära samarbete med övriga berörda myndigheter, kliniska experter, medicintekniska företag och patienter.
Bilden nedan visar processen med det nationella ordnade införandet från horisontspaning till uppföljning.

Ordnat införande av medicinteknik i Region Halland
Region Halland hanterar en rekommendation från MTP-rådet på samma sätt som en rekommendation från Rådet för nya terapier (NT-rådet) gällande läkemedel och nya terapier hanteras.
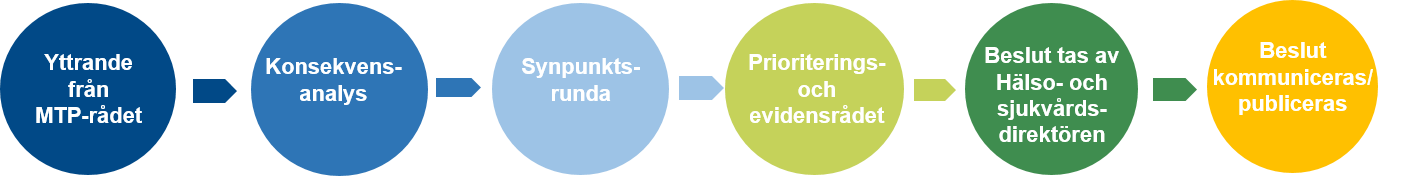
- Nationellt initierade inkomna ärenden behandlas och koordineras av strateg på Regionkontoret.
- Regionala konsekvenser bedöms i samarbete med berörda förvaltningar och dess verksamheter med stöd från bland annat Medicinteknik Halland, Systemförvaltningen och den Centrala funktionen för ekonomi på Regionkontoret. Den sammanställda konsekvensanalysen tillsammans med den nationella rekommendationen sänds på synpunktsrunda till berörda förvaltningschefer.
- Baserat på den nationella rekommendationen, den sammanställda konsekvensanalysen samt förvaltningarnas synpunkter arbetar Prioriterings- och Evidensrådet (PER) fram en rekommendation till beslut.
- Hälso- och sjukvårdsdirektör (HSD) fattar beslut i ärendet.
- Regionkontoret kommunicerar ut beslutet till förvaltningarna via PER. Förvaltningschefen ser till att beslutet förankras i berörda verksamheter.
Produkter som ingår i ordnat införande av ny medicinteknik
Det regionövergripande arbetet fokuserar på nya medicintekniska produkter eller nya metoder som inkluderar medicintekniska produkter för vilka det finns ett behov av att regionerna samverkar för att användningen ska bli kostnadseffektiv, jämlik och ändamålsenlig.
De produkter som kan bli aktuella i den nationella samverkan är medicintekniska produkter som definieras enligt de EU-gemensamma lagstiftningarna för medicintekniska produkter (MDR, Förordning - 2017/745 - EN - EUR-Lex ) och för medicintekniska produkter för in vitro-diagnostik (IVDR, Förordning - 2017/746 - SV - EUR-Lex).
MTP-rådets beslut om nationell samverkan om ordnat införande av nya medicintekniska produkter baserar sig på ett antal prioriteringskriterier för att identifiera de produkter/terapiområden som kan och är mest angelägna att hanteras nationellt med de begränsade resurser som finns till förfogande.
Avgränsning
Det nationellt ordnade införandet omfattar inte medicintekniska produkter/terapiområden som redan är etablerade på marknaden eller nya produkter/terapiområden som inte uppfyller ovanstående prioriteringskriterier.